LAURIL SULFATO DE SÓDIO
PROCESSO PRODUTIVO: FORMULAÇÕES
A síntese do Lauril Sulfato de Sódio é um processo totalmente industrial, sendo que o mesmo não ocorre naturalmente. A substância básica para a sua formação é o álcool láurico, que pode ser obtido pelo óleo de palma ou pelo petróleo. Existem duas formas de síntese do LSS, sendo que ambas são descritas pela patente chinesa CN103058894A [1,3]. Segue abaixo a descrição simplificada destas duas rotas de produção:
1- Em primeiro caso, o SO3 é ligado ao álcool láurico (CH3(CH2)10CH2OH) por uma reação de sulfatação, na qual o álcool é somado a uma solução de trióxido de enxofre (SO3) ou de ácido clorosulfônico (HSO3Cl), gerando o lauril sulfato de hidrogênio, cuja fórmula bruta é C12H25HSO4. Posteriormente à sulfatação, ocorre a neutralização do lauril sulfato de hidrogênio por uma fonte de cátions (como, por exemplo, o hidróxido de sódio (NaOH), o qual se dissocia liberando íons Na+). Esse processo resulta no LSS, substância a qual passa por processos de purificação com um ou mais solventes, como: n-butanol, éter dietílico ou etanol [1,3].
As reações a seguir ilustram quimicamente esse processo:
2- Em uma segunda alternativa, inicia-se a rota de produção por uma reação de sulfatação do álcool láurico (C12H26O) com ácido sulfúrico (H2SO4), resultando em lauril sulfato de hidrogênio. Essa reação deve ser realizada com a adição de uma fonte de cátions (como o carbonato de sódio (Na2CO3), o qual libera íons Na+ quando se dissocia), originando, ao final, o LSS. Posteriormente, o produto é purificado por um ou mais solventes [1,3].
As reações a seguir ilustram quimicamente esse processo:
De um modo simplificado, são essas as formulações químicas para a síntese do LSS [1,3]. Após a escolha do processo mais adequado, será detalhado como ocorre a síntese.
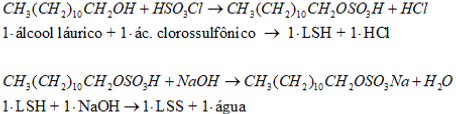

ESCOLHA DO PROCESSO MAIS ADEQUADO
Durante a reação do álcool láurico com o ácido clorossulfônico, sob determinada temperatura, não acontecem reações paralelas (ao contrário do que ocorre na reação do álcool láurico com o trióxido de enxofre gasoso e ácido sulfúrico). Além disso, essa reação tem maior rendimento do que aquela com ácido sulfúrico e o custo do ácido clorossulfônico é menor do que comparado com as outras opções. Por esses motivos, vamos dar continuidade à descrição do processo produtivo com respeito a rota de produção 1 [4,7].
DESCRIÇÃO DO PROCESSO PRODUTIVO (ROTA 1):
O processo descrito abaixo refere-se a uma planta produtiva que utiliza o ácido clorossulfônico para a formação do produto desejado, dado que ele faz uma reação rápida, estequiométrica (1:1) e de custo baixo, comparado ao SO3. Seja um processo em batelada (descrito abaixo), seja um em contínuo (descrito ao final), o processo produtivo do lauril sulfato de sódio ocorre, sinteticamente, em quatro etapas, sendo elas: Sulfatação, Neutralização, Scrubbing e Empacotamento [2,6].
1) Sulfatação:
Dentro de um reator encamisado com vidro borossilicato (para evitar a danificação pelos ácidos) e dotado de agitadores, é colocado o álcool láurico e, aos poucos, adiciona-se o ácido clorossulfônico (HSO3Cl). A reação ocorre a vácuo por duas horas e meia e em temperaturas na faixa de 25 a 30°C para que se evite a formação de substâncias indesejáveis e a oxidação do sistema.
Nessa etapa haverá a produção de lauril sulfato de hidrogênio e ácido clorídrico, como subproduto. Esta substância, obtida em estado gasoso, é imediatamente retirada dos produtos da sulfatação e encaminhada para o sistema de Scrubber (há uma separação de fases nessa etapa). Já o produto principal, lauril sulfato de hidrogênio, é levado para a segunda etapa: a de neutralização [2,5,6].
Segue abaixo a reação química relacionada à esta etapa:
2) Neutralização:
Transfere-se o lauril sulfato de hidrogênio a um vaso de neutralização onde ele entra em contato com uma solução de soda cáustica a 50% (base mássica), juntamente com água. Esse processo é realizado a uma temperatura abaixo de 45 ºC, gerando o lauril sulfato de sódio (separado com a ajuda de um separador orgânico), NaOH diluído e outros subprodutos [2,5,6].
Esta etapa é descrita, com detalhes, pela patente americana (número da patente) e foi com base nela que obtemos as proporções em massa do LSS e dos subprodutos após a neutralização. Segue abaixo as reações químicas que ocorrem nesta etapa, sendo que a primeira é a reação de neutralização propriamente dita do LSH, enquanto que a segunda é a reação de neutralização dos subprodutos que vieram da etapa precedente (como o ácido clorrosulfônico), gerando novos sais [2].
3) Scrubbing:
O ácido clorídrico (HCl(g) ) produzido durante o primeiro processo (sulfatação) é retirado com a ajuda de um pressurizador a vácuo e é levado ao scrubber, máquina responsável pelo processo de lavagem. Tal etapa necessita da adição de uma corrente de água que pode vir em conjunto com um composto alcalino para auxiliar na neutralização do subproduto. Vale ressaltar que o processo é exotérmico e, portanto, requere uma refrigeração para retirada do calor gerado nessa etapa. Isso ocorre através da circulação da solução formada em um trocador de calor externo. Quando a solução atinge grau comercial (entre 32 a 36% em peso de HCl), ela é retirada pelo fundo do scrubber e pode tanto ser reutilizada, quanto levada ao mercado [2,5,6].
4) Embalagem:
Embala-se o LSS em tambores para que posteriormente seja enviado aos armazéns [6].
O processo contínuo ocorre de maneira análoga ao de batelada, seguindo os passos descritos acima, mas com apenas uma diferença: a utilização de um desgaseificador após a reação entre o álcool láurico e o ácido clorossulfônico ter ocorrido no reator. É importante salientar que antes devem ser feitos cálculos para que se saiba sobre as perdas que ocorrem num regime de escoamento. Além disso, a velocidade com que o ácido passa pela tubulação interfere na temperatura com que ele entra na reação, podendo ser um complicador [2,5,6].
Segue abaixo uma ilustração esquemática dos dois processos industriasi (batelada e contínuo):

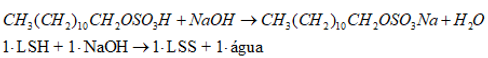

CONTÍNUO

Fonte: (MARCOS; BARCZA, [7])
BATELADA
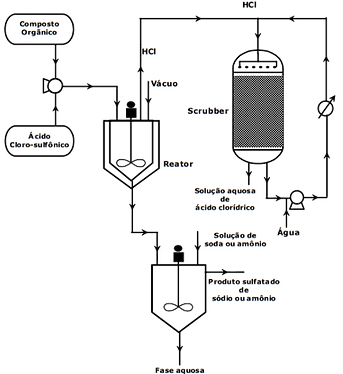
Fonte: (MARCOS; BARCZA, [7])
TENDÊNCIAS DO MERCADO
Segundo estimativas feitas por analistas da Global Market Insights, o valor estimado do mercado de Lauril Sulfato de Sódio em 2018 foi de aproximadamente 550 milhões de dólares [8]. A demanda em países europeus e da América do Norte pelo produto atualmente é a maior. Entretanto, projeções evidenciam um aumento, em escala global do uso do LSS, o que se deve a fatores como:
-
Valorização da indústria de limpeza em países em desenvolvimento (maior relevância de políticas públicas ao saneamento básico);
-
Incremento das preocupações com a higiene (pessoal e comunitária) no período pós pandemia;
-
Crescimento da indústria de cosméticos e cuidados com a pele.
Dados fatores destacados acima, a procura por surfactantes tende a crescer nos próximos anos e, com ela, a oferta desses produtos. Com isso, há a oportunidade para o aumento da capacidade de produção típica, que hoje varia entre 3000 e 21000 toneladas por mês [9], levando-se em consideração a produção das empresas chinesas “Henan Samshande Chemical Products Co., Ltd”, “Henan Bright Commercial Co., Ltd.”, “Henan Win Win Chemical Industrial Co., Ltd.” e “Zhengzhou City Mantanghong Abrasives Co., Ltd.”.
Por conseguinte, em se tratando de um processo industrial de larga escala, a capacidade de produção é algo determinante para a viabilidade de sua fabricação. Empresas com maior poder produtivo são, portanto, as mais competitivas no mercado.
Em relação ao mercado americano, em especial ao brasileiro, a empresa responsável pela produção e distribuição do LSS é a Oxiteno, pertencente ao grupo Ultra [10]. A multinacional nascida na década de 70 está presente em vários países e vem pesquisando e atendendo às necessidades da demanda crescente de produtos químicos. Essa empresa trabalha com 5 segmentos de atuação: coatings, crop solutions, home care and &, oil gas e personal care. Destes 5, o lauril sulfato de sódio está presente em três (crop solutions, home care and & e personal care). Fica evidente, pelos catálogos da empresa, que os segmentos de personal care e home care (cuidados pessoais e cuidados da casa) são os principais a precisarem do LSS em sua composição.
[1] PRODUCTION method of high-purity sodium dodecyl sulfate CN103058894A. Depósito: 24 abr. 2013. Concessão: 1 jul. 2013. Disponível em: https://patents.google.com/patent/CN103058894A/en. Acesso em: 28 abril, 2020.
[2] (SILVIS, 1985)SILVIS, S. J. Neutralization of organic sulfuric or sulfonic detergent acid to produce high solids concentration detergente salt. n. 19, p. 5, 1985. Disponível em: <https://patents.google.com/patent/US4544493A/en>. Acesso em: 28 abril, 2020.
[3] LARROUY, Malaury. Le Sodium Lauryl Sulfate. In: LE SODIUM LAURYL SULFATE, 2015, Université du Québec à Chicoutimi. Le Sodium Lauryl Sulfate [...]. [S. l.: s. n.], 2015. Disponível em: http://www.scc-quebec.org/wp-content/uploads/2017/08/Monographie-Sodium-Lauryl-Sulfate-Malaury-Larrouy-2015.pdf. Acesso em: 15 abr. 2020.
[4] TAKEI, K. et al. Anionic surfactants: lauric products. Journal of the American Oil Chemists’ Society, v. 62, n. 2, p. 341–347, fev. 1985. Disponível em: <https://aocs.onlinelibrary.wiley.com/doi/abs/10.1007/BF02541402>. Acesso em 28 abril, 2020.
[5] FOSTER, N. C. Sulfonation and Sulfation Processes. [s.l: s.n.]. Disponível em: <www.chemithon.com>. Acesso em: 12 maio. 2020.
[6] INTRATEC. Sodium Lauryl Ether Sulfate Production. Sodium Lauryl Ether Sulfate Production - Cost Analysis - SLES E11A, v. 3, p. 13, 2017. Disponível em: <https://www.intratec.us/analysis/report-preview?report=sles-e11a&referer=sppcrfl§ion=executive-summary>. Acesso em: 05 maio. 2020.
[7] MARCOS, P.; BARCZA, V. Sulfatação. [s.d.]. Disponível em: <https://docplayer.com.br/21130820-Sulfonacao-sulfatacao.html>. Acesso em: 28 abril, 2020.
[8] SODIUM Lauryl Sulfate Market Size By Product (Liquid, Dry [Powder, Needles, Granules]), By Application (Dish Washing Liquids, Household Detergents & Cleaners, Industrial Cleaners, Personal Care Products), Industry Analysis Report, Regional Outlook, Growth Potential, Price Trends, Competitive Market Share & Forecast, 2019 – 2026. Disponível em: https://www.gminsights.com/industry-analysis/sodium-lauryl-sulfate-SLS-market. Acesso em: 28 abr. 2020.
[9] Made in China. Factory Price Sodium Lauryl Sulfate/Sodium Dodecyl Sulfate SLS/SDS/ K12 for Cosmetic. In: Factory Price Sodium Lauryl Sulfate/Sodium Dodecyl Sulfate SLS/SDS/ K12 for Cosmetic. [S. l.], 23 ago. 1920. Disponível em: https://samshande.en.made-in-china.com/product/xSLmdEVUuWYJ/China-Factory-Price-Sodium-Lauryl-Sulfate-Sodium-Dodecyl-Sulfate-SLS-SDS-K12-for-Cosmetic.html. Acesso em: 26 abr. 2020
[10] OXITENO: Evolution by chemistry. In: Oxiteno: Evolution by chemistry. c. ed. A: B, 23 abr. 2020. d. Disponível em: http://www.oxiteno.com/webcenter/portal/Oxiteno/oxiteno/documentos?_adf.ctrl-state=12xv6npo58_4&_afrLoop=51297377440058523#!. Acesso em: 28 abr. 2020.